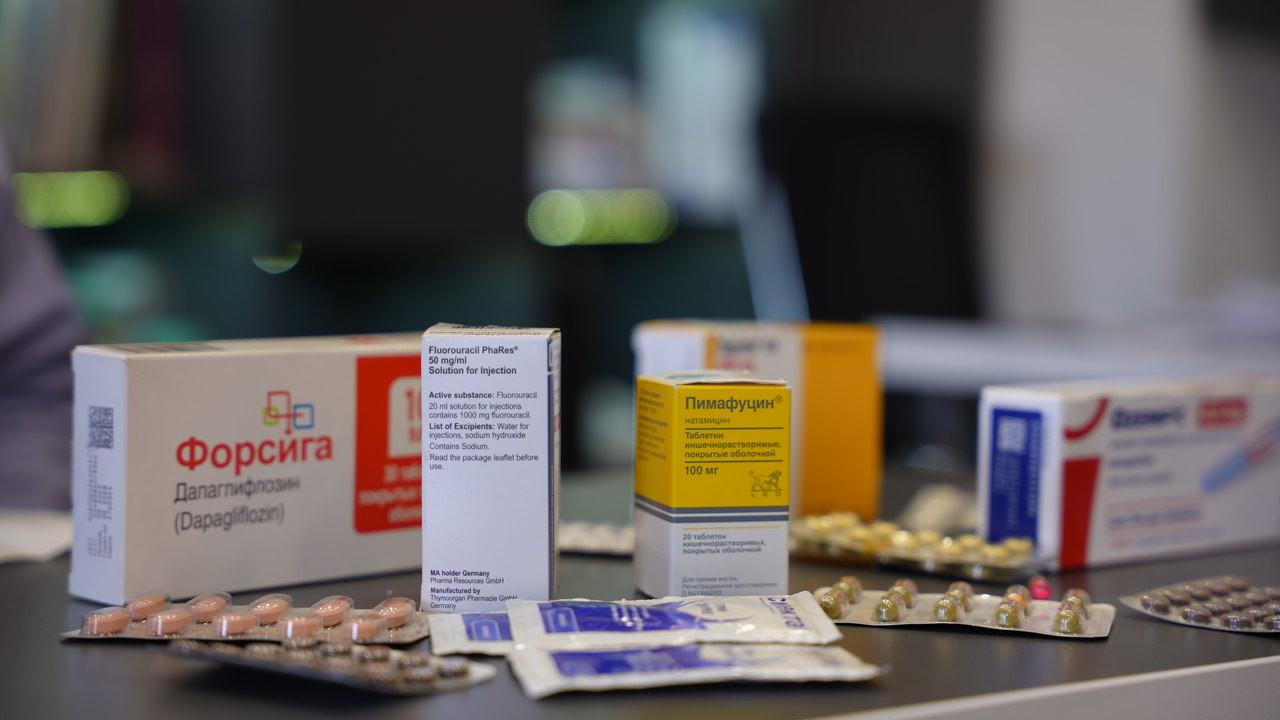
Ինչպես են չգրանցված դեղերը հայտնվում շուկայում
Քաղցկեղի, շաքարային դիաբետի, հորմոնալ խանգարումների և այլ հիվանդությունների բուժման համար նշանակվող բազմաթիվ դեղեր Հայաստանում գրանցված չեն, ուստի չեն կարող օրինական կերպով վաճառվել։ Բայց այդ դեղորայքն ազատ վաճառվում է դեղատներում կամ սեւ շուկայում։ Եվ քանի որ գրանցված չեն, պետական ոչ մի կառույց չի ստուգում դրանց արդյունավետությունն ու անվտանգությունը։ Տարիներ շարունակ բժիշկներն ահազանգում են, որ այդ դեղերը կենսական անհրաժեշտություն են իրենց բուժառուների համար եւ պետք է գրանցվեն ու պատշաճ ստուգում անցնեն՝ բացառելու համար կեղծ դեղերի շրջանառությունը, սակայն պետությունը չի կարողանում լուծել գրանցման հարցը։
«Հետք»-ը դեղատնային ցանցերից մեկի երևանյան և մարզային մասնաճյուղերից ձեռք է բերել Հայաստանում օրինական գրանցում չունեցող 13 դեղամիջոց։ Ցանցի անունը չենք նշում՝ կոնկրետ մեկ ընկերության չթիրախավորելու համար, որովհետեւ չի բացառվում, որ այլ դեղատնային ցանցերում եւս դրանք վաճառվում են։
Ինչու շատ կարևոր դեղեր չեն գրանցվում Հայաստանում
Դեղերի գրանցման գործընթացը Հայաստանում երկար է տևում և թանկ արժե։ Առողջապահության նախարարության տվյալներով՝ ներկայում Հայաստանում գրանցված է 3661 անուն դեղ։ ԱՆ Դեղորայքային քաղաքականության և բժշկական տեխնոլոգիաների վարչության պետ Մարինե Հարությունյանի խոսքով՝ որոշ դեղեր Հայաստան չեն հասնում ոչ թե պետական սահմանափակման, այլ արտադրողի հետաքրքրության բացակայության պատճառով։
«Դեղը գրանցելուց առաջ անցնում է բազմաթիվ հետազոտություններ՝ ինչպես փաստաթղթային, այնպես էլ լաբորատոր փորձաքննություններ։ Եթե այդ բոլոր փորձաքննություններից հետո ունենում ենք դրական եզրակացություն, դրական արդյունքներ, այդ դեպքում նախարարի հրամանով դեղը գրանցվում է 5 տարի ժամկետով»,- ասում է նա։
Հարությունյանի խոսքով՝ Հայաստանի դեղագործական շուկան փոքր է, ինչի պատճառով որոշ արտադրողներ չեն դիմում դեղերը գրանցելու համար։
«Դեղը գրանցողը կամ դեղի իրավատերն է, կամ արտադրողը։ Այսինքն՝ պետք է ներկայացվեն համապատասխան փաստաթղթեր, որոնք տիրապետում է միայն արտադրողը կամ լիազորված իրավատերը։ Մեր շուկայի փոքր ծավալներից ելնելով՝ հաճախ պարզապես հետաքրքրություն չի առաջանում արտադրողների մոտ»,- նշում է նա։
Հարությունյանի խոսքով՝ դեղերի գրանցման մերժումը կախված չէ նախարարության կամ փորձագետի անձնական որոշումից։ «Մերժումները հստակ սահմանված են օրենքով և ենթաօրենսդրական ակտերով։ Եթե կա բացասական եզրակացություն՝ լաբորատոր փորձաքննությունների ոչ գոհացուցիչ արդյունքներ կամ փաստաթղթային թերություններ, և եթե 180 օրվա ընթացքում այդ խնդիրները չեն շտկվել, գրանցումը մերժվում է՝ հիմք ընդունելով օրենսդրական պահանջները»,- բացատրում է նա։
Ոչ օրինական ճանապարհով Հայաստան հասած դեղերի առնչությամբ Հարությունյանը նշում է, թե խնդիրը պայմանավորված է արտադրողների հետաքրքրությամբ. «Եթե արտադրողը պահանջ չի ներկայացնում մեր երկրում գրանցվելու, պետությունը չի կարող պարտադրել։ Բայց մենք օրենսդրական փոփոխություն ենք արել և ունենք հիմնական դեղերի ցանկ, որտեղ ընդգրկված են կենսական անհրաժեշտ դեղեր։ Եթե դեղը կամ դեղաչափը ընդգրկված է այդ ցանկում, ապա նախարարի հրամանով թույլատրվում է ներմուծումը՝ անցնելով փաստաթղթային ուսումնասիրություններ»։
Չգրանցված դեղերի սև շուկայի վերահսկման գործառույթը նախարարությանը վերապահված չէ։ «Առողջապահության նախարարությունը չունի վերահսկողական լծակներ։ Դրանք պատկանում են Առողջապահական և աշխատանքի տեսչական մարմնին, որը համարյա ամենօրյա կտրվածքով ստուգումներ է իրականացնում։ Եթե արձանագրվում է չգրանցված դեղի վաճառք, կիրառվում են բարձր տույժեր և տուգանքներ»,- ասում է նա։
Դեղերի ներմուծմամբ զբաղվելու համար կազմակերպությունը պետք է լիցենզավորված լինի, ունենա պահեստներ, մասնագետներ։ Ներմուծման ընթացքում մաքսային մարմնում և փորձագիտական կենտրոնում իրականացվում են փաստաթղթերի ուսումնասիրություններ։ Այս գործընթացը տևում է 7-10 աշխատանքային օր, որից հետո տրվում է դրական կամ բացասական եզրակացություն։
Նա ընդգծում է, որ օրինական ճանապարհով ներմուծվող չգրանցված դեղերը հիմնականում կենսական նշանակություն ունեն։ «Խոսքը բացառապես օրինական ներմուծման մասին է։ Պետական գնումների միջոցով չգրանցված դեղերի ձեռքբերումը թույլատրվում է ոչ միայն առողջապահության և պաշտպանության նախարարություններին, այլև բուժհաստատություններին։ Սակայն բոլոր չգրանցված դեղերը պետք է արտադրված և գրանցված լինեն ԵԱՏՄ անդամ երկրներում։ Այլ երկրների չգրանցված դեղեր ներմուծել չի թույլատրվում»,-ասում է վարչության պետը։
Սակայն Հայաստանի դեղատներում վաճառվում են դեղեր, որոնք ԵԱՏՄ անդամ երկրների արտադրանք չեն, ոչ էլ Հայաստան են հասել արտոնյալ կարգով՝ նախարարի թույլտվությամբ։
Արդյոք Հայաստանում չգրանցված դեղերի վաճառքը պատշաճ վերահսկվում է հարցին Մարինե Հարությունյանը պատասխանում է․ «Չեմ կարող գնահատական տալ, որովհետև գործառույթը նախարարությանը չէ վերապահված։ Բայց կան հստակ օրենսդրական և ենթաօրենսդրական ակտեր, որոնցով պետք է իրականացվի վերահսկողությունը։ Որքանով որ մենք ենք իրազեկված, այն կատարվում է ամբողջությամբ»։
Ինչպե՞ս են դեղերը վաճառվում դեղատներում
«Հետքը» գնել էր հետեւյալ դեղերը՝
- Օզեմպիկ 0.5 մգ (սերիա՝ PP5N094, պիտանիություն՝ մայիս 2027, գնվել է 2025 թ.-ի օգոստոսի 26-ին։ Դեղն առանց դրոշմապիտակի է, իրացվել է ՀԴՄ կտրոնով)։
- Տեգրետոլ 200մգ (սերիա՝ TLHW5, պիտանիություն՝ հունվար 2027, գնվել է 2025 թվականի հուլիսի 24-ին, ՀԴՄ կտրոնը և դրոշմապիտակն առկա են)։
- Ֆորսիգա 10մգ (սերիա՝ 2720325, պիտանիություն՝ փետրվար 2028, գնվել է 2025 թվականի օգոստոսի 1-ին, ՀԴՄ կտրոնը և դրոշմապիտակն առկա են)։
- Պիմաֆուցին 100մգ հաբ (սերիա՝ 020290, պիտանիություն՝ հոկտեմբեր 2027, գնվել է 2025 հուլիսի 23-ին, ՀԴՄ կտրոնը և դրոշմապիտակն առկա են)։
- Բարալգին (սերիա՝ 4P0563A, պիտանիություն՝ հունվար 2028, գնվել է 2025 թվականի հուլիսի 23-ին, ՀԴՄ կտրոնը եւ դրոշմապիտակն առկա են)։
Դեղի տուփի վրա փակցված դրոշմապիտակի տվյալների վերծանումից պարզվում է, որ ներմուծողը դրոշմապիտակների էլեկտրոնային գրանցման համակարգում տվյալ դեղի հետ ընդհանրապես կապ չունեցող տվյալներ է մուտքագրել. այդ դեղի արտաքին տնտեսական գործունեության ապրանքային անվանացանկի (ԱՏԳԱԱ) կոդի (3004) փոխարեն նշված է չփաթեթավորված վիտամինների կոդ (2936): Հավաստագրման ենթակա ցավազրկող եւ ջերմիջեցնող այս դեղի ապրանքատեսակն էլ ներկայացված է որպես չհավաստագրվող վիտամին:
- Օմնիկ (սերիա՝ 571124, պիտանիություն՝ հուլիս 2028, գնվել է 2025 թվականի հուլիսի 23-ին, ՀԴՄ կտրոնն առկա է, սակայն դրոշմապիտակը բացակայում է)։
- Վեզիկար (սերիա՝ 154378, պիտանիություն՝ ապրիլ 2026, գնվել է 2025 թվականի հուլիսի 23-ին, առանց ՀԴՄ կտրոնի, առանց դրոշմապիտակի)։
- Ալլոխոլ (Фармстандарт, սերիա՝ 740524, պիտանիություն՝ ապրիլ 2028, գնվել է 2025 թվականի հուլիսի 23-ին, ՀԴՄ կտրոնն առկա է, դրոշմապիտակը՝ ոչ)։
- Սմեկտա (սերիա՝ C56167, պիտանիություն՝ ապրիլ 2027, գնվել է 2025 թվականի հուլիսի 23-ին, ՀԴՄ կտրոնն առկա է, դրոշմապիտակը ՝ ոչ)։
- Ատարաքս (սերիա՝ 409451, պիտանիություն՝ հունիս 2029, գնվել է 2025 թվականի հուլիսի 23-ին , ՀԴՄ կտրոնն առկա է, դրոշմապիտակը՝ ոչ)։
- Սենադե (սերիա՝ 484007, պիտանիություն՝ ապրիլ 2027, գնվել է 2025 թվականի հուլիսի 22-ին, ՀԴՄ կտրոնն առկա է, դրոշմապիտակը՝ ոչ)։
12-13. Քսելոդա (սերիա՝ 2408547, պիտանիություն՝ հունիս 2027) և Fluorouracil 50mg/ml (PhaRes, Գերմանիա, սերիա՝ 440700, պիտանիություն՝ հունիս 2026), գնվել են 2025 թվականի օգոստոսի 12-ին, ՀԴՄ կտրոնն առկա է, դրոշմապիտակը՝ ոչ )։
«Հետքը» գնած դեղորայքի ցանկն ուղարկել է Առողջապահության նախարարություն եւ խնդրել հայտնել, թե դրանցից որոնք են հավաստագրված։ Ըստ պատասխանի՝ գնված 13 չգրանցված դեղերից միայն մեկի՝ իտալական «Տեգրետոլ»-ի համար է ներմուծման հավաստագիր տրվել։ «Պիմաֆուցինի» դեպքում նախարարությունը մերժել է ընկերության հայտը, բայց դա խոչնդոտ չի այն վաճառելու համար։ Մեր գնած մյուս 12 դեղամիջոցների վերաբերյալ որեւէ հայտ նախարարության «Թույլատվական փաստաթղթեր» համակարգում չի ներկայացվել։ Այդուհանդերձ, այդ դեղերը հասանելի են մեր այցելած դեղատնային ցանցում։
Դեղերի գրանցման լաբորատոր փորձաքննությունն իրականացնում է Առողջապահության նախարարության ենթակայությամբ գործող Դեղերի և բժշկական տեխնոլոգիաների փորձագիտական կենտրոնը։
Կենտրոնի փոխտնօրեն Նաիրա Ռոմանովայի խոսքով՝ Հայաստանի Հանրապետությունում դեղերը գրանցվում են ընդհանուր և պարզեցված ընթացակարգերով, ինչպես նաև՝ Եվրասիական տնտեսական միության կանոնների համաձայն: Պարզեցված ընթացակարգը կիրառելի է Կառավարության որոշմամբ սահմանված միջազգային մասնագիտական կազմակերպությունների անդամ երկրներում գրանցված կամ ԱՀԿ նախաորակավորված դեղերի համար:
Դեղերի գրանցման ժամանակացույցը կախված է ընթացակարգից: Ազգային ընթացակարգով դեղի պարզեցված գրանցման ժամկետը 31 օր է, իսկ ընդհանուր ընթացակարգով գրանցման առավելագույն ժամկետը 150 օր է: ԵԱՏՄ ընթացակարգով դեղերի գրանցման առավելագույն ժամկետը 180 աշխատանքային օր է:
«Դեղագործական ընկերությունները պետք է պլանավորեն իրենց ներմուծումը՝ հաշվի առնելով գրանցման ժամկետները։ Վերագրանցման դեպքում գործընթացն ավելի կարճ է»,-նշում է փորձագիտական կենտրոնի փոխտնօրեն Նաիրա Ռոմանովան։
Ինչպես են չգրանցված դեղերը շրջանցում մաքսային ծառայությունն ու հայտնվում շուկայում
«Հետքը» Պետական եկամուտների կոմիտեին ներկայացրել է գնված չգրանցված դեղերի ցանկը, դեղատների հասցեներն ու ՀԴՄ կտրոնները։ Դեղերից 3-ի վրա եղել է ՊԵԿ դրոշմապիտակ, այսինքն՝ չնայած դեղը գրանցված չէ, վաճառքը տեղի է ունեցել օրինական հարկային դաշտում։ 12 դեղամիջոցի համար տրամադրվել է ՀԴՄ կտրոն, բոլորի վրա նշված են եղել դեղերի անունները։
ՊԵԿ-ին խնդրել ենք պարզաբանել՝
- Իրացման ժամանակ ՀԴՄ կիրառման կանոնների խախտման դեպքերը, հատկապես՝ առանց ձեռքբերման փաստաթղթերի ՀԴՄ կտրոնների տրամադրումը։
- Նշված դեղերի մի մասի վրա դրոշմապիտակների բացակայության հանգամանքները։
- Որոշ դեղերի պարագայում դրոշմապիտակների առկայության օրինականությունը։
ՊԵԿ-ը հայտնել է, որ թեմատիկ հարկային ստուգում կանի և արդյունքների մասին կտեղեկացնի։ Թե ինչ ժամկետում հայտնի չէ։
Բարձր ռիսկերով շուկա, թույլ վերահսկողություն
Դեղերի շրջանառությունը վերահսկում է Կառավարությանն առընթեր Առողջապահական և աշխատանքի տեսչական մարմինը։ Տեսչական մարմնի տվյալներով՝ 2024 թվականին ստուգվել է 199 դեղ ներմուծող եւ վաճառող տնտեսվարող, կազմվել է 160 ակտ, 838 իրավախախտման դեպքով կիրառվել է վարչական պատասխանատվություն։
Դեղերի շրջանառության վերահսկողության վարչության պետ Նարեկ Կարապետյանը նշում է, որ հայտնաբերվում են չգրանցված կամ օրենքի խախտմամբ ներմուծված դեղեր, տրվում են կարգադրագրեր՝ խմբաքանակը ոչնչացնելու վերաբերյալ։ Եթե տնտեսվարողը չի կատարում հանձնարարականը, ենթարկվում է վարչական պատասխանատվության։
Բացի պլանային ստուգումներից, գործում է նաև հսկիչ գնման մեխանիզմ։ Կառավարության որոշմամբ սահմանվել է կարգ, ըստ որի՝ հսկիչ գնումը կատարվում է տեսչական մարմնի ղեկավարի հանձնարարագրով։ Երբ արձակվում է հանձնարարագիրը, տվյալ տնտեսվարողի մոտ սկսվում է հսկիչ գնում, որից անմիջապես հետո՝ ստուգում»։
Մեր հարցին, թե ինչն է հիմք հանդիսանում հսկիչ գնում իրականացնելու համար՝ բողո՞ք, զա՞նգ, թե կասկածելի տվյալներ, Նարեկ Կարապետյանը նշում է. «Հսկիչ գնումն իրականացվում է միայն ստուգումների շրջանակներում՝ ըստ օրենքի։ Եթե կազմակերպությունը ներառված է տարեկան ստուգումների ցանկում, ապա կարող է իրականացվել նաև հսկիչ գնում։ Եթե տեսչական մարմնում որևէ տեղեկատվություն է մուտք լինում, դիմում կամ բողոք, ապա հարուցվում է վարչական վարույթ, կատարվում են զննումներ, և անհրաժեշտության դեպքում դեղերն ուղարկվում են փորձագիտական կենտրոն՝ պարզելու՝ ներմուծումը և գրանցումը կատարվե՞լ են օրենքի համաձայն, թե ոչ»։
Դեղատները վճարում են տուգանքը և շարունակում վաճառել չգրանցված դեղերը։ Եթե որևէ բողոք կամ ահազանգ չլինի, վերահսկողությունը կրկնվելու է լավագույն դեպքում հաջորդ տարի՝ ստուգումների ցանկում ընդգրկվելու դեպքում։ Այսինքն՝ անգամ տուգանվելուց հետո տնտեսվարողը չի զրկվում չգրանցված դեղը վաճառելու հնարավորությունից։
Առողջապահության նախարարության, Տեսչական մարմնի և ՊԵԿ-ի գործողությունները ցույց են տալիս, որ դեղերի շուկայում վերահսկողությունը թերի է։ Առողջապահական համակարգը վերահսկող երեք հիմնական կառույցները գործնականում քիչ են համագործակցում։ Այդ բացը հնարավորություն է տալիս չստուգված դեղերն ազատ վաճառել։ Անգամ տուգանքներից հետո վաճառքը չի դադարում։ Այսինքն՝ վարչական տուգանքները զսպող միջոց չեն, հատկապես, որ այդ դեղերի կարիքը կա։ Ուրեմն պետությունը պետք է գտնի ձեւը՝ կենսական անհրաժեշտություն համարվող դեղերը գրանցելու, որպեսզի դեղատները խախտումների չդիմեն, իսկ հիվանդները կարողանան որակյալ դեղորայք օգտագործել։
 Տեսանյութեր
Տեսանյութեր Լուսանկարներ
Լուսանկարներ
Մեկնաբանություններ (1)
Մեկնաբանել